代谢综合征、肥胖以及糖尿病等葡萄糖代谢障碍(Glucose metabolism disorders)疾病,已经成为全球范围内日益严峻的公共健康问题。越来越多研究表明,肠道微生态系统——尤其是肠道菌群——在调节宿主能量代谢和血糖稳态方面发挥重要作用。然而,在这个复杂生态系统中,还有一个与细菌数量相当却长期被忽视的重要成员:肠道病毒组。过去二十年的微生物研究几乎都集中在肠道菌群,而肠道中大量存在的病毒,特别是噬菌体,一直缺乏系统研究。宏基因组学研究曾发现,肥胖或糖尿病患者的肠道病毒组的组成往往发生明显变化。但这些研究大多停留在“相关性”层面:病毒组的改变究竟是疾病的结果,还是可能参与了疾病的发生发展?这一关键问题一直缺乏直接证据。
针对这一问题,韦德1946体育官方入口附属金陵医院李维勤教授与浙江大学动物科学学院付爱坤教授团队开展了一系列系统研究,试图回答一个悬而未决的问题:肠道病毒组是否能够像细菌组一样,直接调控宿主的代谢过程?
研究团队首先关注人体营养吸收最关键的部位——小肠。小肠不仅负责大部分宏量营养素的消化和吸收,也是人体共生病毒组最大的居住地。那么,小肠对碳水化合物的感知和消化吸收,是否可能受到肠道病毒组的影响?
在高碳水化合物饮食喂养的小鼠模型中,研究人员使用抗病毒药物降低肠道病毒载量,结果发现小鼠的代谢状态随之发生改变:体重增加、饲料利用效率下降,同时口服葡萄糖耐量明显受损。进一步分析发现,小肠上皮细胞中多种与碳水化合物消化吸收相关的基因表达显著上调。为了排除肠道细菌的干扰,研究团队采用了多种严格控制的实验体系,包括不同来源的SPF小鼠、抗生素消化道去污小鼠,甚至无菌小鼠模型。结果显示,无论小鼠原本的细菌群组成如何,只要降低肠道病毒载量,都会出现类似的碳水化合物代谢异常。相反,如果向无菌小鼠移植共生病毒组,则能够逆转这一效应,恢复正常代谢状态,并抑制小肠中相关消化吸收基因的过度表达。进一步实验还表明,无论是模式噬菌体,还是来源于人类或小鼠肠道的原代噬菌体,都能够模拟病毒组的代谢调节作用,而且这种作用呈现明显的剂量依赖性。
这些结果首次表明:肠道病毒组本身就可以独立于细菌,直接参与调控宿主的碳水化合物代谢。
那么,病毒组是如何影响宿主代谢的呢?研究团队进一步解析了其中的分子机制。实验发现,肠道病毒对小肠碳水化合物吸收的调控实际上具有一种“油门—刹车”式的双重作用——当免疫系统缺乏正常监视时,病毒核酸可以直接刺激肠上皮细胞,使其上调碳水化合物消化吸收相关基因,从而增强糖分吸收——这相当于踩下了“油门”;而在免疫系统健全的情况下,情况则完全不同。研究发现,肠道病毒会被小肠黏液层中的抗原呈递细胞摄取,并通过MHCII通路激活CD4+T细胞。这些T细胞进一步诱导Th17细胞产生关键细胞因子IL-22。IL-22作用于肠上皮细胞后,可以抑制因病毒核酸刺激而过度激活的碳水化合物消化吸收程序,从而限制糖分过量吸收——这一过程相当于代谢调控中的“刹车”。
因此,肠道病毒组对宿主代谢的最终影响,取决于一个关键条件:肠道免疫系统是否保持完整的监视功能。
通过这一系列研究,团队首次系统性地描绘出一条完整的生物学通路:肠道共生病毒组 →免疫感知→IL-22信号→上皮细胞响应→代谢稳态调控
这一发现不仅揭示了肠道病毒组在宿主代谢调控中的全新角色,也为理解肠道共生病毒组与肥胖、糖尿病等代谢性疾病之间的关系提供了重要的因果证据。
这一基础研究的突破,也为未来的临床治疗带来了新的想象空间。面对全球日益严峻的糖尿病和肥胖问题,现有治疗手段往往侧重于抑制淀粉酶或改善胰岛素敏感性。而本研究提示,肠道病毒组本身也可作为一个可调控的重要变量。未来,通过调控肠道病毒组的丰度或特定组成,或许能够从源头影响糖分吸收,从而为代谢性疾病的预防和治疗提供新的思路。例如,筛选特定“益生噬菌体”或者特定病毒成分“益生噬菌体元”,作为靶向小肠IL-22 信号通路的精准药物,都有可能成为未来代谢疾病干预的新策略。某种意义上,这一研究不仅深化了“肠道菌群”这一概念,也让我们意识到:在人类肠道这片微观生态系统中,病毒同样可能是维持健康的重要参与者。随着对肠道病毒组认识的不断深入,这场发生在微观世界中的“生态博弈”,或许将为我们理解宏观健康与疾病打开新的窗口。
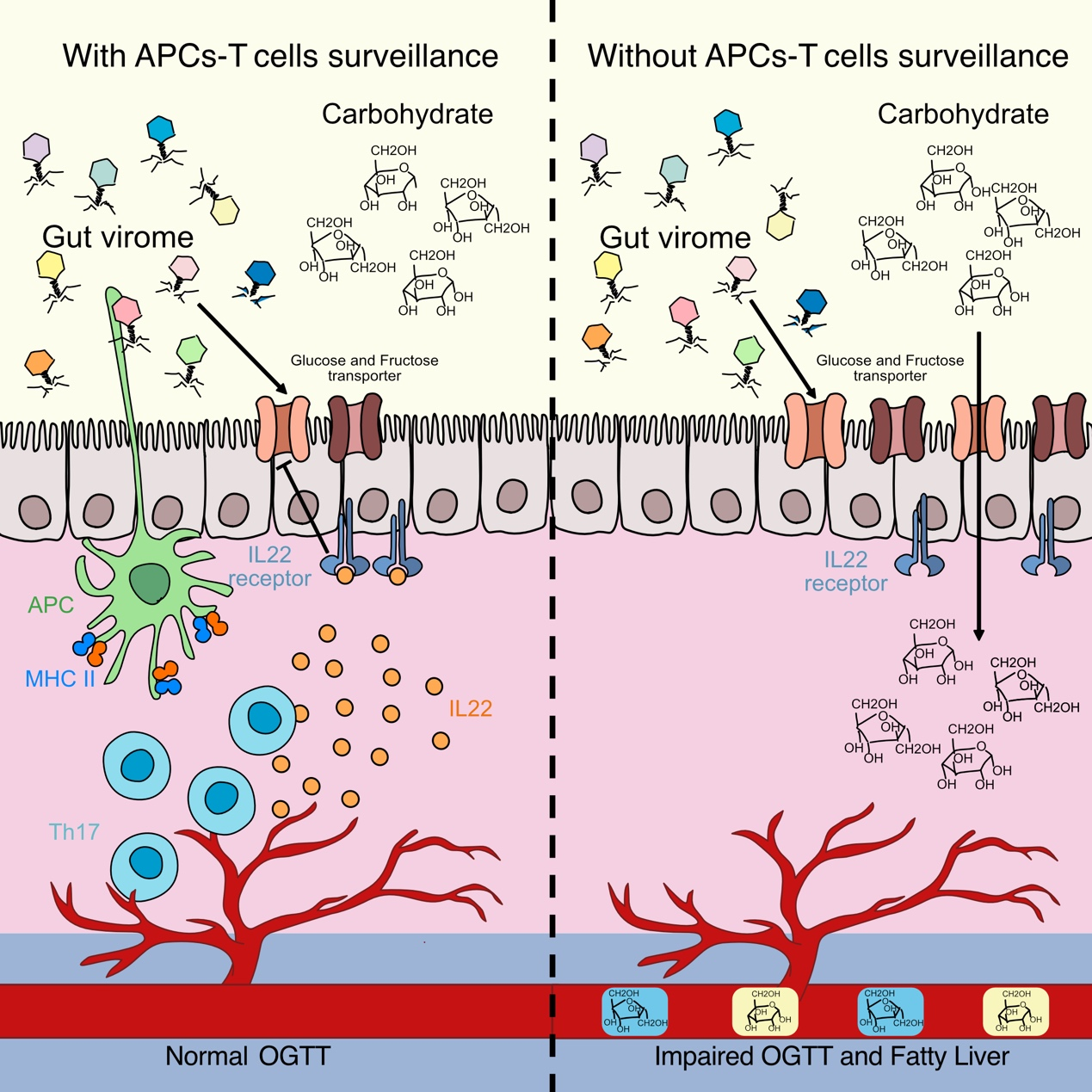
图1.肠道病毒组通过APC-Th17-IL-22轴调控小肠碳水化合物代谢机制图
2026年2月,该研究成果以长文形式正式发表于Cell子刊《Cell Host and Microbe》杂志。韦德1946体育官方入口附属金陵医院李维勤教授与浙江大学动物科学学院付爱坤研究员为论文共同通讯作者,韦德1946体育官方入口2022级博士研究生林峰庆与2023级博士研究生李梁岚为论文共同第一作者。

原文链接:https://www.cell.com/cell-host-microbe/fulltext/S1931-3128(26)00044-2
